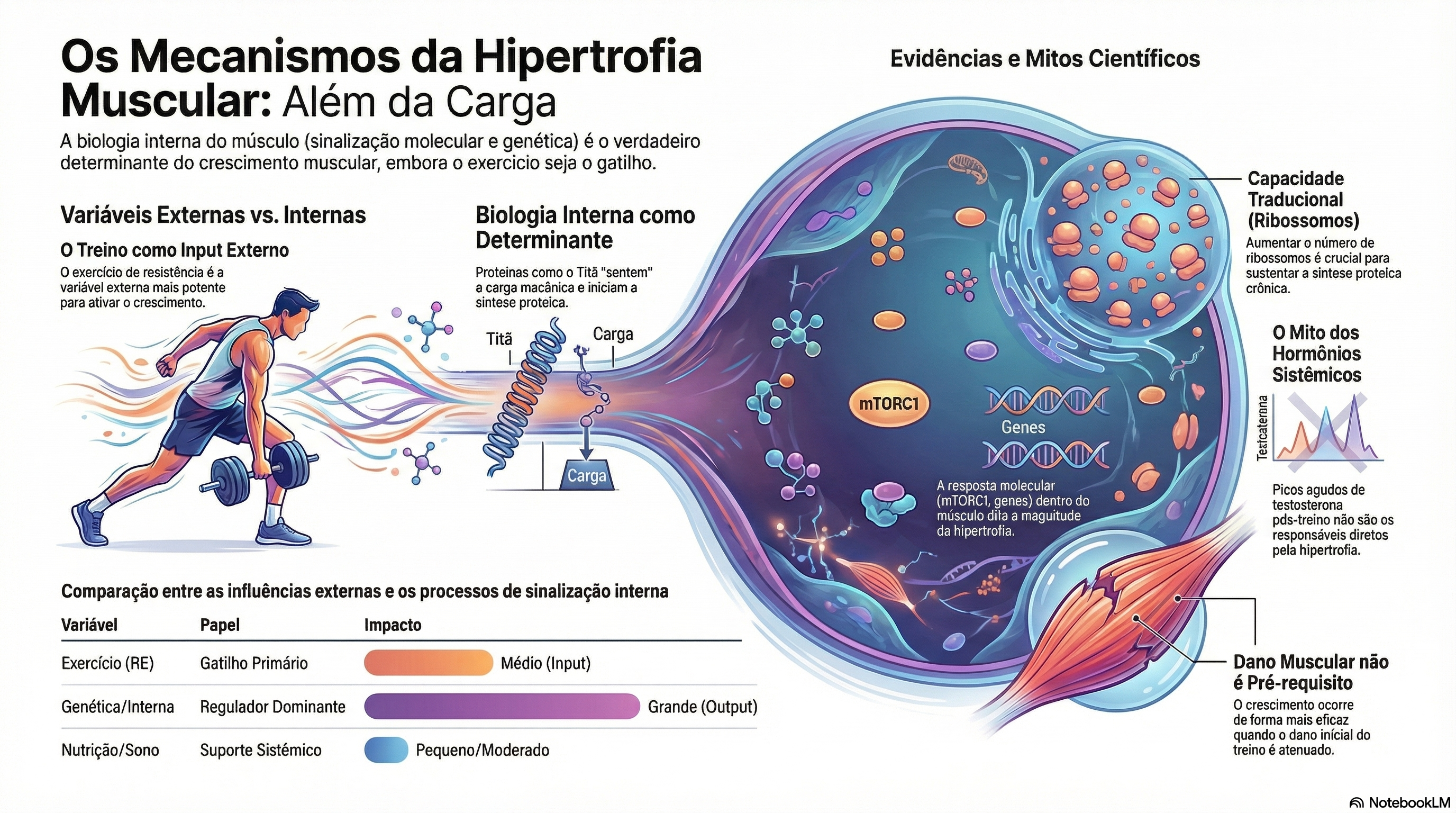
O artigo de Lim, Nunes, Currier, McLeod, Thomas e Phillips é uma revisão narrativa fundamentada em evidências, e não um estudo experimental original. Seu objetivo central é reorganizar a discussão sobre hipertrofia muscular a partir de uma distinção conceitual relevante entre variáveis externas e internas. As variáveis externas incluem, por exemplo, o treinamento resistido, a dieta, o sono e alguns suplementos. As variáveis internas correspondem aos processos biológicos próprios do músculo esquelético, como mecanotransdução, sinalização intracelular, biogênese ribossomal, respostas transcricionais e participação de células satélite. A tese defendida pelos autores é clara: embora o treinamento resistido seja o principal estímulo externo não farmacológico para promover hipertrofia, a magnitude final do crescimento muscular parece depender sobretudo da resposta das variáveis internas a esse estímulo. Em outras palavras, não basta aplicar carga; é a forma como o tecido muscular traduz essa carga em sinal biológico que define a adaptação.
Esse enquadramento teórico aparece de modo didático já na Figura 1, na página 2, em que a hipertrofia é apresentada como produto da interação entre “input” externo e “output” biológico mediado por processos internos. O ponto mais importante dessa formulação é que o treinamento não é tratado como causa mecânica direta e isolada do aumento de massa muscular, mas como um gatilho que aciona mecanismos celulares específicos. Essa posição desloca o foco de explicações simplistas, centradas apenas em carga, volume ou na resposta hormonal aguda, para um modelo em que o músculo é entendido como um tecido que interpreta sinais mecânicos, nutricionais e moleculares.
No nível molecular, os autores lembram que hipertrofia é definida como aumento da área de secção transversa do músculo ou da fibra muscular e ocorre por acúmulo de proteínas celulares em fibras já existentes. Nesse contexto, um princípio básico permanece válido: para haver hipertrofia, a síntese proteica muscular deve exceder a degradação proteica, de modo a produzir balanço proteico líquido positivo. O artigo ressalta, no entanto, que ainda há lacunas importantes sobre quais adaptações estruturais exatamente acompanham o aumento da massa muscular em humanos, o que impede afirmações excessivamente categóricas sobre a arquitetura final do músculo hipertrofiado.
Entre os mecanismos analisados, a mecanotransdução ocupa posição central. Os autores descrevem o exercício resistido como um estímulo mecânico que impõe carga ao músculo, mas destacam que ainda não se conhece de forma completa como essa carga é “sentida” pela fibra e convertida em sinal anabólico. Nessa discussão, aparecem estruturas como a matriz extracelular, os costâmeros, a focal adhesion kinase, a fosfolipase Cγ1, o ácido fosfatídico e os efetores da via HIPPO, YAP e TAZ. A proposta é que esses elementos componham parte do sistema sensor que traduz deformação mecânica em resposta bioquímica. O texto também menciona titina e o complexo Filamin C Bag3 como candidatos relevantes nesse processo, embora reconheça explicitamente que vários desses vínculos ainda não estão plenamente esclarecidos em humanos. Portanto, a relevância da mecanotransdução é alta, mas o campo permanece mecanisticamente incompleto.
A revisão dedica atenção especial à via mTOR, talvez a rota anabólica mais conhecida no contexto do treinamento resistido. A conclusão, contudo, é mais cuidadosa do que frequentemente se divulga. Os autores aceitam que a ativação do mTORC1 tem papel importante no aumento da síntese proteica muscular, mas ressaltam que isso não resolve sozinho a explicação da hipertrofia. Um ponto particularmente importante é que o aumento agudo da síntese proteica após uma sessão isolada de exercício nem sempre se correlaciona com a hipertrofia crônica observada após semanas de treinamento. O artigo cita evidências de que, nas fases iniciais do treinamento, parte relevante desse aumento agudo da síntese proteica pode estar mais relacionada ao reparo e à remodelação de dano do que propriamente ao crescimento muscular sustentado. Com a continuidade do treinamento, a associação entre síntese proteica pós exercício e hipertrofia tende a se tornar mais consistente. Além disso, a revisão destaca a possibilidade de mecanismos sensíveis e insensíveis à rapamicina participarem conjuntamente da resposta hipertrófica, sugerindo que reduzir toda a discussão ao mTOR seria biologicamente insuficiente.
A Figura 2, na página 4, sintetiza bem esse cenário ao mostrar que múltiplas vias convergem sobre a síntese proteica. Nutrientes, sinais mecânicos e fatores de crescimento interagem com reguladores como PI3K, Akt, TSC, Rheb, ERK1/2 e diversos alvos translacionais. A imagem reforça uma conclusão decisiva da revisão: a hipertrofia não decorre de uma única “chave” molecular, mas de uma rede integrada de sinalização. Isso enfraquece leituras reducionistas que tentam explicar a adaptação apenas por um marcador isolado, como p70S6K, testosterona ou lactato.
Outro eixo importante do artigo é a biogênese ribossomal. O raciocínio aqui é que aumentar a massa muscular não depende apenas de ativar a maquinaria de síntese proteica já existente, mas pode exigir também expansão da capacidade translacional da célula, isto é, aumento do conteúdo ribossomal. Os autores explicam que a síntese proteica pode subir tanto por maior eficiência translacional quanto por maior capacidade translacional. A revisão sustenta que a biogênese ribossomal emergiu como um regulador plausível da hipertrofia induzida pelo treinamento resistido, sobretudo em fases iniciais do processo adaptativo. Ainda assim, o texto é prudente: em humanos treinados, o conteúdo total de RNA nem sempre aumenta de forma mensurável após uma sessão de exercício, e diversos marcadores de transcrição ribossomal parecem estabilizar após poucas semanas. Isso levou os autores a sugerir que a resposta inicial pode envolver expansão relativamente rápida da maquinaria translacional, seguida por uma fase em que a eficiência do sistema se torna mais importante do que sua expansão contínua.
A Figura 3, na página 5, é particularmente esclarecedora nesse ponto. Ela propõe um modelo temporal em que a síntese proteica muscular se eleva de forma acentuada no início do treinamento, em paralelo a maior capacidade translacional, para sustentar remodelação estrutural e contratil. Com o passar das semanas, a contribuição do dano muscular diminui, a resposta torna-se mais específica ao estímulo e a eficiência translacional passa a predominar. O crescimento da fibra aparece como resultado acumulado desse processo. Trata-se de uma formulação relevante porque corrige a ideia de que toda elevação aguda de síntese proteica significa, automaticamente, construção líquida de massa muscular.
Apesar disso, o artigo reconhece que a literatura sobre biogênese ribossomal e hipertrofia crônica ainda não é conclusiva. Há heterogeneidade interindividual importante, inclusive em aspectos como número de cópias de rDNA e expressão de pré rRNA, e parte dos estudos disponíveis carece de grupo controle ou de desenho capaz de separar variação biológica real de erro aleatório. Assim, a revisão não afirma que maior biogênese ribossomal explique de forma definitiva quem hipertrofia mais, mas propõe que essa é uma das hipóteses mais promissoras para pesquisa futura.
Na seção sobre expressão gênica, o artigo apresenta um panorama compatível com a literatura moderna de “omics”. O exercício pode alterar a abundância de mais de 2000 transcritos, mas os autores alertam que grandes quantidades de genes diferencialmente expressos não significam, por si sós, explicação causal da hipertrofia. Uma crítica importante feita pela revisão é que muitos estudos transcriptômicos descreveram mudanças moleculares sem incorporar, de forma robusta, a mudança fenotípica central de interesse, isto é, o crescimento muscular propriamente dito. Quando essa associação é feita, surgem achados mais úteis. Os autores citam um conjunto de 141 genes correlacionados à remodelação muscular induzida por carga em humanos e destacam um resultado especialmente interessante: alterações no comprimento das regiões não traduzidas do mRNA, as UTRs 3’ e 5’, mostraram associação estreita com ganho de massa muscular, mesmo quando a abundância total do mRNA não se alterava. Além disso, processos ligados a remodelação da matriz extracelular, angiogênese e função mitocondrial apareceram como eixos centrais do crescimento muscular.
Esse ponto é cientificamente relevante porque sugere que a regulação da hipertrofia não depende apenas de “mais transcrição”, mas também de como os transcritos são processados, estabilizados e traduzidos. O artigo, portanto, amplia a discussão para além da velha oposição entre “mais carga” e “mais hormônio”, posicionando a hipertrofia como fenômeno dependente de regulação fina da maquinaria celular.
A seção sobre hormônios anabólicos sistêmicos é uma das mais contundentes da revisão. Os autores sustentam, com base em vários estudos, que os aumentos agudos e transitórios de testosterona, GH e IGF 1 após o exercício resistido não parecem ter papel mecanístico causal relevante na hipertrofia. O texto destaca que essas elevações duram tipicamente 15 a 30 minutos e permanecem dentro ou próximas da variação fisiológica diária, muito distantes das concentrações atingidas por administração exógena farmacológica. O artigo cita evidências de ausência de associação entre essas respostas hormonais agudas e aumento de síntese proteica muscular ou hipertrofia crônica. Em contraste, o conteúdo de receptor androgênico no próprio músculo surge como variável potencialmente mais informativa.
A Figura 4, na página 7, ilustra esse contraste de forma didática ao comparar a pequena elevação transitória de testosterona induzida por uma sessão de exercício com concentrações muito mais elevadas e duradouras após administração exógena. A mensagem é direta: não é cientificamente adequado equiparar o pico hormonal fisiológico pós treino ao efeito anabólico de exposições farmacológicas. A revisão ainda acrescenta um argumento adicional de grande peso: mulheres e homens apresentam ganhos relativos semelhantes de força e hipertrofia com treinamento resistido, apesar das mulheres terem concentrações circulantes de testosterona muito menores. Isso é difícil de conciliar com a hipótese de que a testosterona sistêmica aguda seja determinante central da hipertrofia induzida pelo treino.
Quanto ao estrogênio, o tom é mais cauteloso. O artigo admite plausibilidade biológica para um papel protetor ou modulador, inclusive por reduzir dano muscular e interagir com vias anabólicas, mas afirma que ainda não há consenso. Assim, o tratamento dado a esse hormônio é de hipótese em investigação, e não de mecanismo estabelecido.
A revisão também questiona um dos dogmas mais repetidos na área do treinamento: a ideia de que dano muscular seja pré requisito para hipertrofia. O texto mostra que, embora o dano induzido pelo exercício aumente marcadores inflamatórios e estimule células satélite, medidas indiretas como creatina quinase e dor muscular não se correlacionam bem com síntese proteica muscular nem com hipertrofia. Em indivíduos destreinados, esses marcadores tendem a ser maiores no início do treinamento, justamente quando o sistema ainda está se adaptando ao estímulo. Com a continuidade do programa, o dano cai progressivamente, mas a hipertrofia pode seguir ocorrendo. O artigo ainda cita evidências de que parte do reparo local pode ocorrer independentemente de células satélite, por mecanismos relacionados à migração nuclear dentro da própria fibra. Em síntese, a revisão não nega que dano e inflamação participem da remodelação muscular, mas rejeita a noção de que mais dano implique necessariamente mais hipertrofia.
Em linha semelhante, os autores examinam a hipótese de que metabólitos como lactato, íons hidrogênio, fosfato inorgânico e queda de fosfocreatina seriam grandes indutores diretos de crescimento muscular. A conclusão é negativa. Embora esses metabólitos se elevem intensamente durante contrações musculares, a revisão afirma que não há evidência causal robusta mostrando que eles sejam sinais anabólicos primários em humanos. O artigo lembra ainda que exercícios que produzem concentrações metabólicas altas, como sprints ou esforços intervalados intensos, não promovem hipertrofia do mesmo grau que o treinamento resistido. Além disso, em estudos citados pela revisão, a restrição de fluxo sanguíneo não gerou hipertrofia adicional em comparação ao treinamento resistido tradicional, e aumentos de lactato plasmático não produziram incremento adicional de síntese proteica ou de área de secção transversa muscular. Portanto, a interpretação final é que metabólitos podem acompanhar o exercício, mas não se sustentam como motores centrais da hipertrofia.
Do ponto de vista clínico, a revisão amplia a discussão para doença e envelhecimento. Os autores destacam que o treinamento resistido não deve ser tratado como ferramenta exclusiva de atletas ou fisiculturistas. Em diversas condições clínicas, como câncer, DPOC, doença cardiovascular, sepse, doença renal e Parkinson, a perda muscular decorre, ao menos em parte, de maior degradação proteica, menor ativação de vias anabólicas, inflamação sistêmica e redução drástica da atividade física. Nesse cenário, o treinamento resistido pode aumentar massa magra ou, em muitos casos, ao menos mitigar a perda muscular. Os autores chamam atenção para um ponto conceitual importante: em populações clínicas, muitas vezes o efeito observado é melhor descrito como atenuação da atrofia do que como “hipertrofia verdadeira” no sentido clássico.
No envelhecimento, o artigo relaciona a sarcopenia a fatores como inflamação crônica de baixo grau, perda de proteostase, redução da capacidade regenerativa, denervação parcial e resistência anabólica. Ainda assim, a revisão afirma que o treinamento resistido permanece como estímulo consistente para melhorar força e atenuar a perda de massa muscular associada à idade. A Figura 5, na página 10, resume fatores que contribuem para essa resistência anabólica e inclui um elemento que os autores tratam como especialmente importante: episódios periódicos de desuso. Isso tem implicação prática clara. Para além da composição do treino, evitar longos períodos de inatividade parece ser componente decisivo da preservação muscular ao longo da vida.
Na conclusão, o artigo adota uma posição equilibrada. A revisão reconhece o mTOR como peça central do anabolismo muscular, mas sustenta que esse componente não esgota a explicação da hipertrofia. Entre os mecanismos mais promissores para investigação futura em humanos, os autores destacam mecanotransdução, capacidade translacional, eficiência translacional e regulação transcricional. Também apontam que técnicas mais recentes, como quantificação in vivo de síntese de rRNA, isolamento de célula única e single cell RNA seq, podem acelerar a identificação de assinaturas moleculares mais específicas do crescimento muscular. A Figura 6, na página 10, sintetiza essa visão integrativa ao reunir mecanotransdução, sinalização intracelular, ribossomos, UTRs de mRNA, receptor androgênico, inflamação e envelhecimento em um mesmo esquema conceitual.
Do ponto de vista da divulgação científica, a principal contribuição desta revisão é desfazer explicações excessivamente simplificadas sobre hipertrofia. O artigo sustenta que o crescimento muscular não pode ser atribuído de forma convincente nem aos picos agudos de hormônios sistêmicos, nem ao dano muscular por si só, nem ao acúmulo de metabólitos isoladamente. O cenário descrito é mais complexo e, ao mesmo tempo, mais biologicamente plausível: a hipertrofia depende de como o músculo converte tensão mecânica em sinais intracelulares, organiza sua maquinaria translacional, remodela sua expressão gênica e responde ao treinamento de forma progressivamente mais específica ao longo do tempo. Em termos práticos, isso favorece uma leitura menos espetacularizada do fenômeno e mais coerente com a fisiologia contemporânea.
Referência
Lim C, Nunes EA, Currier BS, McLeod JC, Thomas ACQ, Phillips SM. An Evidence-Based Narrative Review of Mechanisms of Resistance Exercise–Induced Human Skeletal Muscle Hypertrophy. Medicine & Science in Sports & Exercise. 2022;54(9):1546-1559.